Atom Karbon & Senyawa Karbon – Karbon adalah sebuah bagian yg paling banyak didapatkan di muka bumi. Bahkan unsur tersebut dapat membentuk berbagai senyawa yg berlawanan.
Di dlm kerak bumi, bagian karbon
ditemukan dlm keadaan bebas maupun dlm bentuk senyawanya, terutama berupa
mineral karbonat. Unsur karbon pula mampu didapatkan di dlm tubuh makhluk
hidup yg kemudian disebut senyawa karbon organik.
Selain itu, karbon pula dapat
didapatkan dlm bentuk senyawa anrganik. Sebagai acuan, gas karbon dioksida
yang merupakan gas yg tak beracun. Gas karbon dioksida salah satunya
dihasilkan dr hasil pembakaran & pernafasan.
Daftar Isi
Allotrop Karbon
Karbon mempunyai tiga allotrop (bentuk-bentuk yg berbeda & berasal dr satu komponen yg sama). Ketiga allotrop atom karbon ialah grafit, intan, & karbon amorf.
Grafit berwarna hitam & mudah ringkih yg dibuat melalui arang. Kegunaan grafit adalah selaku elektroda untuk baterai maupun elektrolisis. Sedangkan arang ialah teladan karbon yg stabil yg kadang-kadang dipakai sebagai materi bakar.
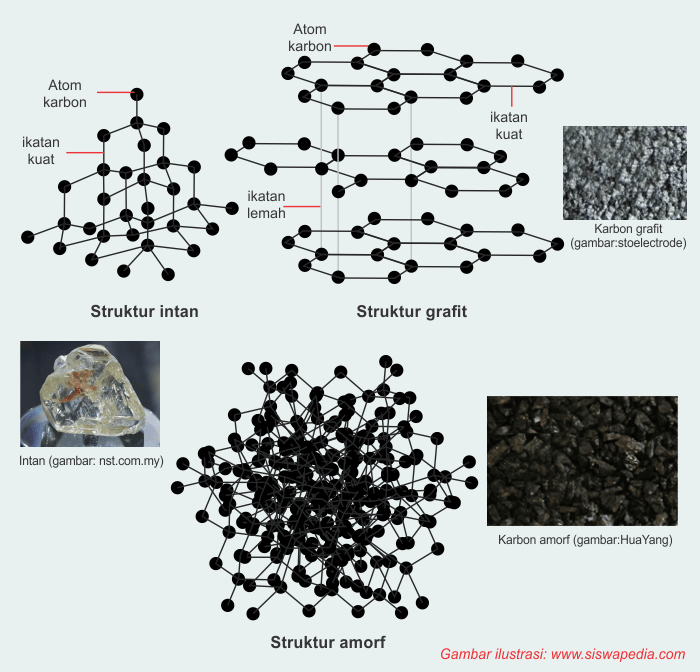
Intan merupakan bentuk lain dari
karbon, meski warnanya sama-sama kehitaman tetapi mempunyai struktur yg berbeda
dengan grafit. Intan banyak dipakai sebagai pelengkap maupun selaku pemotong
di bidang industri alasannya sifatnya yg keras. Karbon amorf dapat didapatkan
pada kokas, abu karbon, arang tulang, maupun arang kayu.
Karbon banyak didapatkan di kerikil
bara, salah satu hasil tambang yg digunakan selaku bahan bakar. Melalui
proses destilasi kering, watu bara tersebut bisa dimurnikan hingga menjadi
kokas. Kokas biasanya dipakai selaku reduktor pada pengolahan aneka macam macam
logam.
Kekhasan Atom Karbon yg Tidak
Dimiliki Unsur Lain
Atom karbon memiliki beberapa sifat khas yg diketahui dlm ilmu kimia. Beberapa sifat khas dr atom karbon ialah selaku berikut.
1. Dari tabel periodik bagian kita dapat mengenali bahwa atom karbon dgn lambang C memiliki nomor atom & jumlah elektron sebanyak 6. Itu artinya atom karbon mempunyai elektron valensi sebanyak 4. Keempat elektron valensi tersebut dapat membentuk pasangan elektron bareng dgn atom-atom yg yang lain. Ikatan ini disebut dgn ikatan kovalen.
2. Keempat elektron valensi atom karbon dapat membentuk rantai tersendiri. Sehingga akan dihasilkan banyak sekali kemungkinan terbentuknya senyawa-senyawa yg berlawanan. Kemungkinan ini didasarkan pada jenis ikatan, jumlah ikatan, serta posisi atom karbon tersebut di dlm rantai karbon.
3. Karbon pula mampu membentuk rantai lurus, bercabang, maupun siklik.
4. Selain itu karbon dapat membentuk ikatan kovalen melalui ikatan tunggal & ikatan rangkap.
Senyawa-senyawa Karbon
Karena unsur karbon mempunyai kemampuan untuk membentuk banyak sekali senyawa yg berbeda. Untuk mempermudah pembelajaran ilmu kimia khususnya tentang senyawa karbon, senyawa-senyawa tersebut dikelompokkan berdasarkan gugus fungsi yg terikat pada karbon. Pada biasanya, senyawa ini disebut pula selaku senyawa hidrokarbon.
Artikel terkait: Tata nama senyawa organik
Adapun pengelompokkan senyawa karbon
yaitu alkana, alkena, alkuna, eter, ester, asam karboksilat, alkohol, keton,
aldehid, & haloalkana. Alkana, alkena, & alkuna yakni senyawa karbon yang
dibedakan menurut jenis ikatan (ikatan rangkap & ikatan tunggal).
Senyawa akohol mempunyai gugus
hidroksil yaitu –OH. Sedangkan senyawa haloalkana mengikat atom halogen mirip
F, Cl, Br, & I. Kemudian untuk senyawa eter, karbon mengikat oksigen sehingga
disebut dgn gugus alkoksi.
Selain itu, senyawa keton mengikat gugus karbonil begitu juga dgn aldehid. Perbedaannya yaitu, pada keton, oksigen di apit oleh dua atau lebih karbon.
Sedangkan pada aldehid, gugus karbonil berada di ujung dr rantai karbon. Asam karboksilat memiliki gugus fungsi –COOH sedangkan ester mempunyai gugus fungsi –COO-
Bila ada pertanyaan terkait postingan atom karbon & senyawa karbon di atas, bisa ditulis di bawah ini.
Sumber :
Brady, J.E. (1999). Kimia Universitas: Asas & Struktur jilid
1, Edisi ke 5. Terjemahan Sukmariah Maun, Karnianti Anas & Tilda S.
Sally. Binarupa Aksara: Jakarta.