Daftar Isi
Konsep Kimia Dasar: Dunia Kimia, Klasifikasi Materi dan Reaksi Kimia
Oleh Aryo Gusman ( @V08-Aryo )
Ilmu kimia ialah ilmu yang mempelajari wacana komposisi, sifat fisik dan kimia, pergantian materi serta energi yang menyertai pergeseran tersebut. Komposisi (susunan) zat menyatakan perbandingan bagian pembentuk zat itu. Sebagai acuan, air dan etanol yang dirumuskan H2O dan C2H5OH. Struktur zat kimia menggambarkan letak atom-atom dalam ruang 3 dimensi. Gambar 1 di bawah ini ialah teladan untuk struktur air dan etanol.
Dunia Kimia
Dalam dunia kimia yang sudah disepakati oleh para ahli, terbagi menjadi 3 dunia yaitu dunia makroskopik, submikroskopik dan simbol
1. Makroskopik
Makroskopik adalah pengamatan fenomena kimia yang mampu dilihat langsung atau persepsi eksklusif yang dialami oleh seseorang dari percobaan di laboratorium atau kehidupan sehari-hari. Contohnya pergeseran warna, terbentuknya gelembung gas, terbentuknya endapan, pelarutan garam, pH larutan dan perubahannya, adanya spektrum cahaya, dan pergeseran suhu dalam reaksi kimia.
2. Submikroskopik
Submikroskopik yaitu sesuatu yang tidak kasat mata lewat pendekatan konsep teori ilmiah dalam bidang kimia yang mampu digunakan untuk menerangkan susunan serta pergerakan partikel (ion, elektron, molekul, dan atom).
3. Simbol
Simbol merupakan representasi yang melibatkan penggunaan simbol-simbol kimia secara kualitatif dan kuantitatif, yang mencakup rumus kimia, persamaan reaksi, bentuk gambar, diagram, aljabar, grafik, prosedur reaksi, simbol kimia, struktur kimia, nomor, stoikiometri, perhitungan matematik, analogi dan model kit
Gambar 2. Tiga Dunia Kimia
Sifat & Perubahan Materi
Perubahan zat kimia dapat terjadi secara alami maupun sebab perlakuan manusia. Untuk mampu mengetahui zat tersebut, dapat dilaksanakan identifikasi melalui sifat-sifat dan susunannya.
a. Sifat fisika
Sifat yang menyebabkan pergantian secara fisik bahan, contohnya warna, rasa, kekerasan, kelarutan, kerapatan, titik leleh, titik didih dan lain-lain.
b. Sifat kimia
Sifat yang memiliki kemampuan untuk mengalami pergantian atau reaksi secara kimiawi. Contohnya ialah kestabilan, daya ionisasi, kereaktifan.
Perubahan materi mampu dikasifikasikan menjadi 2, yaitu perubahan fisika dan pergantian kimia.
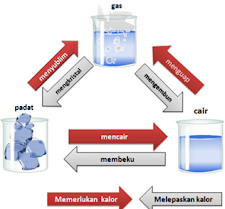
a. Perubahan fisika disebabkan oleh ulah insan, dimana hal ini tidak membuat suatu zat menciptakan zat gres tanpa mengubah susunan suatu zat. Perubahan fisika akan menciptakan pergantian bentuk/wujud suatu zat alasannya adalah adanya dampak perubahan suhu/temperatur lingkungan. Berdasarkan gambar 3, pergantian fisika mampu dirangkum menjadi 6 insiden diantaranya membeku, mencair, menyublim, menguap, mengembun dan mengkristal
b. Perubahan kimia ialah pergeseran yang hendak menghasilkan zat gres. Pembakaran kayu merupakan salah satu teladan pergeseran kimia yang sering kita temui sehari-hari. Kayu termasuk dalam benda organik, sehingga ketika kayu dibakar akan menghasilkan reaksi H2O dan CO2. Pembakaran tersebut akan membuat zat gres yang berbentukarang kayu.
Wujud Materi
Materi yakni segala sesuatu yang menempati ruang dan memilik massa. Dalam hal ini, bahan memiliki 3 wujud yakni padat, cair, dan gas. Ketiga wujud ini dapat bermetamorfosis wujud yang lain.
a. Zat Padat, benda kaku dengan bentuk tetap mempunyai molekul yang terstruktur dan gaya tarik menarik antar molekul kuat. Contoh : bolpoin, penghapus, buku, papan tulis, es watu
b. Zat Cair, memiliki volume yang tetap dan bentuk berganti-ubah sesuai dengan tempatnya serta mempunyai molekul yan kurang terorganisir. Contoh : air, minyak goreng, bensin, spirtus
c. Zat Gas, memiliki bentuk dan volume yang tidak tetap
Klasifikasi Materi
Zat merupakan materi yang berisikan susunan tertentu atau tetap dan memiliki sifat-sifat tertentu. Materi terbagi menjadi zat murni dan adonan, yang mana zat murni digolongkan menjadi komponen dan senyawa.
1. Zat Murni/zat tunggal
a. Unsur
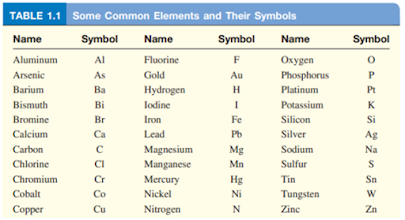
Salah satu golongan dari zat murni yang tidak mampu diuraikan kembali menjadi zat lain yang lebih sederhana dengan cara kimia. Unsur senantiasa ditandai dengan abjad kapital pada huruf pertama lambang, contohnya Na yaitu lambang untuk Sodium, Zn yakni lambang untuk Zinc. Untuk lebih jelasnya dapat dilihat pada Gambar 4 dibawah ini:
b. Senyawa
Zat tunggal yang terdiri dari dua unsur atau lebih, mempunyai komposisi yang tetap sehingga dapat diuraikan dengan cara kimia. Setiap senyawa memiliki sifat yang berbeda dengan unsur pembentuknya, sehingga hanya bisa diuraikan menjadi komponen-unsur pembentuknya melalui reaksi kimiawi. Senyawa berisikan senyawa organik dan anorganik.
1) Senyawa organik ialah senyawa yang terbentuk oleh makhluk hidup atau organisme, mengandung karbon dan hidrogen serta bagian yang lain seperti nitrogen dan oksigen. Oleh alasannya adalah itu CO, CO2 dan O2 bukanlah senyawa organik sebab tidak mengandung hidrogen.
2) Senyawa anorganik merupakan senyawa yang tidak terbentuk dari karbon. Contoh: Natrium Klorida (NaCl), Oksigen (O2), Karbondioksida (CO2), Asam Nitrat (HNO3), Asam Klorida (HCl) dan lain-lan.
2. Campuran
Gabungan antara dua atau lebih zat tunggu dengan perbandingan yang tidak tetap atau sembarang. Campuran terbagi menjadi dua, yakni homogen dan heterogen. Misalnya saat gula dilarutkan dalam air, susunannya diseluruh bagian larutan akan sama. Inilah yang disebut dengan adonan homogen. Untuk adonan heterogen, mampu diambil pola air dan minyak, debu kopi dan gula. Campuran tersebut mampu berbentuklarutan, koloid maupun suspensi.
Untuk melakukan pemisahan adonan, dapat melalui proses fisika maupun kimia bergantung dengan jenis, sifat dan wujud komponennya. Campuran berwujud padat dan cair mampu dipisahkan dengan saringan. Kemudian untuk adonan homogen, mirip alkohol dalam air dapat dipisahkan dengan cara destilasi, rekristalisasi, ekstraksi dan kromatografi.
Reaksi Kimia
1. Reaksi Pembakaran
Reaksi dengan bahan yang gampang terbakar dengan pengoksidasi untuk menghasilkan produk yang teroksidasi. Contoh: 2Mg + O2 → 2MgO + Panas
Reaksi di mana dua atau lebih reaktan bergabung untuk membentuk satu produk tunggal diketahui selaku reaksi kombinasi.
Contoh: 2Na + Cl2 → 2NaCl
3. Reaksi Dekomposisi (Penguraian)
Reaksi dimana satu senyawa terurai menjadi dua atau lebih senyawa yang lebih sederhana
Contoh: CaCO3 → CaO + CO2
4. Reaksi Perpindahan
Contoh: Zn + CuSO4 → ZnSO4 + Cu
5. Reaksi Perpindahan Ganda (Metatesis)
Reaksi perpindahan ganda terjadi di mana ion dipertukarkan antara dua reaktan yang membentuk senyawa gres.
Bentuk persamaan: XY + ZA → XZ + YA
Contoh: BBaCl2 + Na2SO4 → BaSO4 + 2NaCl
6. Reaksi Presipitasi
Reaksi kimia yang melibatkan pembentukan produk yang tidak larut (endapan; padatan)
Referensi
http://repo.stkip-pgri-sumbar.ac.id/id/eprint/3855/1/Kimia%20Dasar-Ratulani.pdf
http://repository.uhamka.ac.id/id/eprint/1238/1/BUKU%20AJAR%20KIMIA%20DASAR%20FIX.pdf
https://rumushitung.com/2016/12/03/pergantian-fisika-dan-perubahan-kimia/
https://www.gramedia.com/literasi/reaksi-kimia/